नमस्कार दोस्तों, आज के इस पेज पर हम आवर्त सारणी की समस्त जानकारी पढ़ने वाले हैं तो इस आर्टिकल को पूरा जरूर पढ़िए।
पिछले पेज पर हमने कार्बन की जानकारी शेयर की हैं तो इस आर्टिकल को भी पढ़े चलिए आज के इस पेज पर हम आवर्त सारणी की समस्त जानकारी को पढ़ते और समझते हैं।
आवर्त सारणी क्या हैं
यह रासायनिक तत्वों की एक तालिका है जो परमाणु संख्या के क्रम में इस प्रकार व्यवस्थित है कि समान परमाणु संरचना वाले तत्व ऊर्ध्वाधर स्तंभ में प्रदर्शित होते हैं।
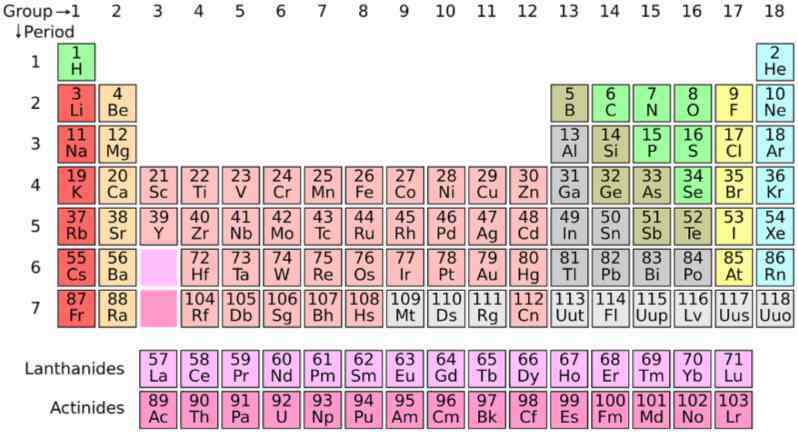
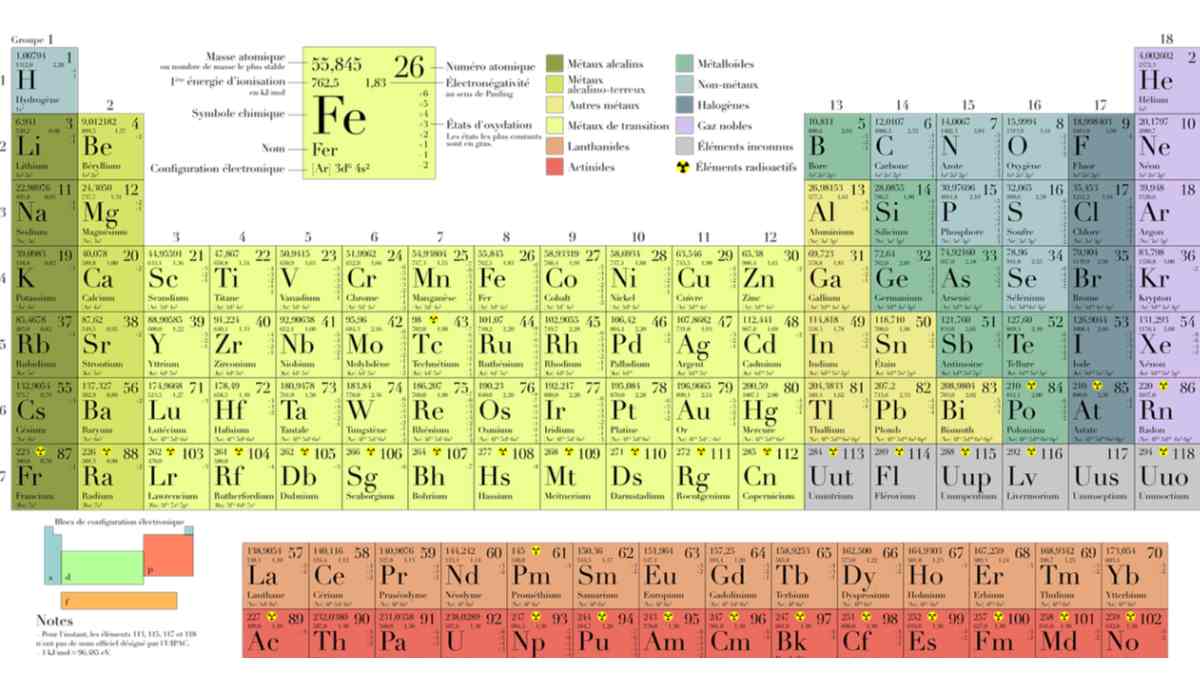
आधुनिक आवर्त नियम : आधुनिक आवर्त नियम कहता है “तत्वों के रासायनिक एवं भौतिक गुण-धर्म उनके परमाणु संख्याओं के आवर्ती फलन होते हैं”। आधुनिक आवर्त सारणी (चित्र 1) आधुनिक आवर्त नियम पर आधारित है।
आधुनिक आवर्त सारणी की प्रमुख विशेषताएँ
आधुनिक आवर्त सारणी को आवर्त सारणी का दीर्घ रूप भी कहते हैं। इसमें 18 वर्ग (ग्रुप) तथा 7 आवर्त (पिरियड) हैं।
वर्ग
किसी एक वर्ग के सभी तत्त्वों के परमाणुओं के सबसे बाहरी कक्षा में इलेक्ट्रानों की संख्या (अर्थात ‘संयोजक इलेक्ट्रानों’ की संख्या) समान होती है। इस कारण किसी एक वर्ग के सभी तत्वों के मुख्य गुण समान होते हैं।
हल्की धातुएँ – वर्ग 1 और 2
अल्कली धातुएं – वर्ग 1
अल्कलाइन मृदा धातुएं – वर्ग 2
भारी धातुएँ या संक्रमण धातुएँ’ – वर्ग 3, 4, 5, 6, 7, 8, 9, 10, 11 और 12
अधातुएँ – वर्ग 13, 14, 15, 16 और 17
खण्ड या ब्लॉक
संयोजक इलेक्ट्रानों के आधार पर तत्वों को 4 खण्डों में बाँटा गया है – s, p, d, f
s-block – वर्ग 1 तथा 2
p-block – वर्ग 13 से 18
d-block – वर्ग 3 से 12
f-block – लैन्थेनाइड और ऐक्टिनाइड (Lanthanide and Actinide series)
प्रतिनिधि तत्व (Representative Elements या Normal elements या Typical elements) – s-block और p-block के तत्वों को सम्मिलित रूप से
संक्रमण तत्व (Transition Elements) – d-block के तत्व
अन्तरिक संक्रमण तत्व (Inner Transition Elements) – f – block के तत्त्व – इन्हें विरल मृदा तत्व (Rare Earth Elements) भी कहते हैं।
आवर्त
- प्रथम आवर्त में केवल 2 तत्त्व हैं, यह सबसे छोटा आवर्त है।
- दूसरे और तीसरे आवर्त में आठ-आठ तत्त्व हैं। इन्हें ‘लघु आवर्त’ (short period) कहते हैं।
- चौथे और पाँचवें आवर्त में 18-18 तत्त्व हैं। इन्हें ‘दीर्घ आवर्त’ कहते हैं।
- छठे आवर्त में 32 तत्त्व हैं। यह सबसे बड़ा आवर्त है।
- सातवाँ आवर्त अपूर्ण है।
- छठे आवर्त के तीसरे वर्ग में परमाणु क्रमांक 57 से 71 तक के तत्त्व हैं। इन्हें ‘लैन्थेनाइड’ कहते हैं।
- सातवें आवर्त के तीसरे वर्ग में परमाणु क्रमांक 89 से 103 वाले तत्त्व हैं। इन्हें ऐक्टिनाइड (actinides) कहते हैं।
संबंधित शब्दावलियां :
1. परमाणु संख्या :- किसी तत्व की परमाणु संख्या उस तत्व के परमाणु के नाभिक में मौजूद प्रोटोन की संख्या होती है।
2. द्रव्यमान संख्या :- किसी तत्व की द्रव्यमान संख्या उस तत्व के परमाणु के नाभिक में मौजूद न्यूट्रॉन की संख्या होती है।
3. परमाणु द्रव्यमान :- परमाणु द्रव्यमान किसे परमाणविक कण, उप-परमाणविक कण, या नाभिक का द्रव्यमान होता है।
4. इलेक्ट्रॉनिक विन्यास :- इलेक्ट्रॉनिक विन्यास, परमाणविक या आणविक कक्षाओं में किसी परमाणु के इलेक्ट्रॉनों का वितरण है।
5. गलनांक :- वह तापमान जिसपर कोई तत्व अपनी अवस्था को ठोस से द्रव में बदलता है उसे तत्व का गलनांक कहते हैं।
6. क्वथनांक :- वह तापमान जिसपर द्रव का वाष्प दाब द्रव के आसपास के दाब के बराबर हो जाता है और द्रव वाष्प में परिवर्तित हो जाता है उसे उस तत्व का क्वथनांक कहते हैं।
तत्वों का वर्गीकरण :
वर्ग 1 में, जिसका स्थान सबसे बाईं ओर होता है, उसमें क्षारीय धातु रहते हैं (Li, Na, K, Rb, Cs और Fr)।
क्षारीय मृदा धातु वे धात्विक तत्व होते हैं जो आवर्त सारणी के वर्ग 2 में पाए जाते हैं।
आवर्त सारणी के मध्य भाग में वर्ग 3 -12 में पाए जाने वाले तत्व संक्रमण तत्व कहलाते हैं। संक्रमण तत्वों में, संयोजी इलेक्ट्रॉन एक से अधिक शेल में मौजूद होते हैं।
कुछ मामूली अपवाद के साथ, संक्रमण धातु परमाणुओं की इलेक्ट्रॉनिक संरचना को [ ]ns 2 (n-1)d m के रूप में लिखा जा सकता है, जहां आंतरिक d कक्षा में संयोजी-शेल s कक्षा की तुलना में अधिक ऊर्जा होती है।
वर्ग 18 में, जिसका स्थान सबसे दाईं ओर होता है, आदर्श गैसें होती हैं (He, Ne, Ar, Kr, Xe और Rn)। उनके सबसे बाहरी शेल्स में 8 इलेक्ट्रॉन होते हैं।
He को छोड़कर, क्योंकि इसका बाहरी शेल होता है K और इसमें अधिकतम 2 इलेक्ट्रॉन ही रह सकते हैं।
आंतरिक संक्रमण तत्व :
परमाणु संख्या 58 से 71 (Ce से Lu) वाले 14 तत्व लैंथेनाइड्स कहलाते हैं और उन्हें तत्व लैंथेनम (La), समान अवस्थिति (आवर्त 6 में वर्ग 3) में परमाणु संख्या 57, के साथ रखा जाता है क्योंकि उनके बीच बहुत अधिक समानता है। हालांकि, सुविधा के लिए, उन्हें मुख्य आवर्त सारणी के नीचे अलग से दिखाया जाया है।
परमाणु संख्या 90 से 103 (Th से Lr) वाले 14 तत्व ऐक्टिनाइड्स कहलाते हैं और उन्हें तत्व लैंथेनम (Ac), समान अवस्थिति (आवर्त 7 में वर्ग 3) में परमाणु संख्या 89, के साथ रखा जाता है क्योंकि उनके बीच बहुत अधिक समानता है। उन्हें भी मुख्य आवर्त सारणी के नीचे लैंथेनाइड्स के साथ दिखाया जाता है।
FAQ
Ans. मेंडलीफ
Ans. 18 वर्ग और 7 आवर्त
Ans. ओगनेसन (Og)
Ans. तत्वों के गुण उनकी परमाणुता के आवर्त फलन होते हैं।
Ans. 1869 में रूसी रसायनज्ञ मेँडलीव ने आवर्त सारणी का निर्माण किया।
Ans. आवर्त सारणी में हाइड्रोजन ‘सबसे हल्का और और पहला तत्व’ है।
उम्मीद हैं आपको आवर्त सारणी की जानकारी पसंद आयी होगी। यदि आपको यह जानकारी पसंद आयी हो तो अपने दोस्तों के साथ सोशल नेटवर्क पर शेयर जरूर करें।